产品背景:
临床输液反应以热原反应危害最大,发生率最高。内毒素(即革兰氏阴性菌细胞壁的脂多糖分子,lipopolysaccharide,LPS)是研究最透彻也是最常见的生物热原,注射即使是pg级别的内毒素,也会导致病人严重的热原反应,引起人体发热、休克甚至死亡。内毒素普遍存在且不易灭活,对制药和医疗器械行业是一个挑战。因此,灵敏可靠的内毒素分析技术是非常必须的。
海鲎的阿米巴样细胞(amoebocytes)对LPS具有超强敏感性,利用海鲎血液阿米巴样细胞溶解物制成鲎试剂的内毒素检测方法自上世纪70年代中期开始应用于医药领域,很快被世界各国广泛采用并将其定为法定的细菌内毒素检查法。经过几十年的发展和改良,鲎试剂内毒素检测法已应用于制药、医疗器械、水质、食品检测以及科研等各大领域。
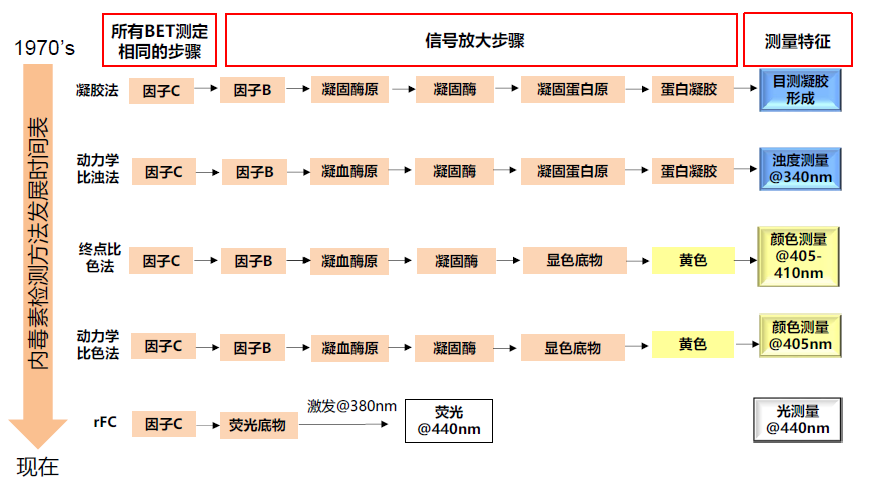
图1. 鲎试剂检测方法的发展和改良历史
采用成分复杂的海鲎血液细胞裂解物作为反应原料具有无法克服的缺陷。例如:
1. 非特异性干扰问题:鲎试剂除了能与内毒素反应外,还会与(1-3)-β-D-葡聚糖反应,造成假阳性结果;
2. 批次稳定性问题:鲎试剂采用海鲎血液作为生产原料,由于季节、地域等差异,使得鲎试剂的批次差异成为常见现象;
3. 鲎资源生态保护需求:环境污染等原因造成海洋中鲎数量种群的减少导致原材料越来越难以获得;
4. 医药行业日益增长的需求和有限的鲎资源的供需不平衡:随着人用和动物用注射药物(如化学药品、放射性药物、抗生素类、生物制品等)及医疗器械(如透析液、植入式器械等)需求迅速增长。
因此开发快捷而可靠的定量检测内毒素的替代方法变得越来越重要。
产品概述:
鲎C因子是鲎血细胞中一种对细菌内毒素敏感的丝氨酸蛋白酶原,在细菌内毒素介导的鲎血凝集系统中,鲎C因子第一个被内毒素激活而启动整个鲎血细胞中的血凝级联反应。Rhinogen® 重组C因子是以基因重组的方式表达的东方鲎(Tachypleus tridentatus) C因子重组蛋白(Recombinant Factor C, rFC),通过内毒素结合并激活的重组C因子能够切割底物获得游离的荧光基团,荧光基团的释放与内毒素的浓度呈正比,从而使得内毒素被定量检测。与经典的鲎试剂内毒素检查方法相比,重组C因子内毒素检测法具有更高的特异性,更好的专属性、精密度、准确度、线性范围及定量限,是目前鲎试剂内毒素检测方法的改良方法。
产品规格:
Rhinogen® 重组C因子内毒素检测试剂盒包装规格如下:
注:本试剂盒含有足够进行96 tests(96孔板:100μl/孔/test)的试剂)
试剂盒组分
货号
规格
RAF-02
96tests
荧光底物试剂
RAF-01B
6ml
测定缓冲液
RAF-01C
5ml
rFC酶溶液
RAF-01D
0.6ml×2
无热原水
RAF-01E
30ml
96孔平底可拆卸微孔板
(白底透明盖)
RA-HC02
1个
产品特性:
Rhinogen® 重组C因子内毒素检测试剂盒是一种不依赖于动物源性成分,灵敏度高、特异性高、可稳定且持续提供的替代鲎试剂的内毒素测定产品,具有如下特性:
1. 单步,终点荧光测定;
2. 检测时间只需90min;
3. rFC液体试剂,操作更方便;
4. 标准96孔板中检测,操作方便,且高通量;
5. 灵敏度范围大:0.005EU/ml~5EU/ml;
6. 内毒素特异性,无G因子旁路干扰,避免结果出现假阳性;
7. 消除了对动物源试剂的依赖,且符合3R的替代原则,提供更高的供应安全性;
8. 重组表达生产,产品批间一致性良好。
本试剂盒可替代传统鲎试剂用于人用和动物用注射药物(如化学药品、放射性药物、抗生素类、生物制品等)及医疗器械(如透析液、植入式器械等)的原辅材料、中间产品、放行产品的内毒素检测。
保存条件:
采用冰袋运输。收到试剂盒后,请立即置于2℃~8℃储存。未开封产品有效期为12个月。